Lebermetastasen sind Töchtergeschwülste (Absiedelungen = Filiae) bösartiger Tumoren, die ihren Ursprung in anderen Organen haben. Dabei treten häufig Absiedelungen von Dick- oder Enddarmkarzinomen (Kolon- oder Rektumkarzinom) auf. Die Zahl der Neuerkrankungen in Deutschland mit Absiedelungen von Darmtumoren in der Leber werden auf ca. 28.000 pro Jahr geschätzt. Sie können aber auch aus Lungen-, Magen-, Bauchspeicheldrüsenkarzinomen und vielen anderen Tumoren (z.B. GIST, NET, Melanom, Brustkrebs usw.) hervorgehen. Die Absiedelungen treten entweder zusammen mit dem Ursprungstumor auf (synchron), oder entstehen erst im weiteren zeitlichen Verlauf (metachron). Unter Einbeziehung einer begleitenden Chemotherapie lassen sich viele kolorektale Metastasen aber auch neuroendokrine (NET) und gastrointestinale stromatumoröse (GIST) Absiedelungen in der Leber durch vollständige chirurgische Entfernung gut therapieren. Absiedelungen von anderen Karzinomen aus Magen oder Bauchspeicheldrüse (Pankreas) zeigen eine weniger gute Ansprechrate auf die Therapie (siehe Tab 1). Bei der Prognoseeinschätzung und Entscheidung für oder gegen eine Operation (Metastasenresektion) spielen neben dem Ursprungsort des Tumors bei den nichtkolorektalen/nichtneuroendokrinen Lebermetastasen allerdings auch das Alter des Patienten, die Anzahl und Ausdehnung der Metastasen, der zeitliche Abstand des Auftretens zwischen Ursprungstumor (Primarius) und Lebermetastase und die leberisolierte Absiedelung eine wesentliche Rolle. Somit muss bei diesen Tumoren die Operationsindikation zur Metastasenentfernung als Einzelfallentscheidung im Rahmen unseres interdisziplinären Tumorboardes besprochen werden.

Tabelle 1.: Prognose nach Resektion (Entfernung) von Lebermetastasen unterschiedlicher Tumore bzw. Karzinome (=Ca) (nach Adam R. et al., Association Francaise de Chirurgie (AFC) 2011).
Chemotherapie bei Lebermetastasen
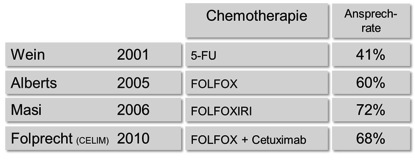
Durch neue Chemotherapeutika und deren kombinierten Einsatz mit altbewährten Substanzen konnten insbesondere beim kolorektalen Karzinom in den letzten Jahren deutliche Fortschritte erzielt werden. Dies führt nicht nur dazu, dass bei nicht operablen Befunden ein längeres Überleben erzielt werden kann, sondern auch, dass eine medikamenten-induzierte Tumorschrumpfung von anfänglich nicht entfernbaren zu operablen bzw. resektablen Lebermetastasen führen kann, wie die Ansprechraten verschiedener Chemotherapieregime in Abb.1 unterstreichen.
Abb. 1: Tumor – Ansprechraten (Tumorschrumpfung) in Abhängigkeit des verwendeten Chemotherapieregimes (modifiziert nach Steger/Germer 2012)
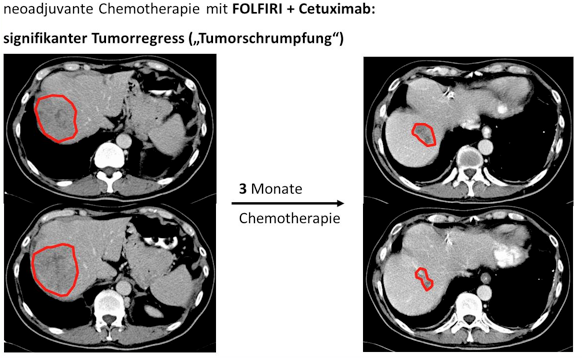
Insbesondere der Einsatz von modernen Antikörpern wie Cetuximab oder Bevacizumab, die gegen Wachstumsrezeptoren der Tumorzellen gerichtet sind, hat zur erheblichen Steigerung der Ansprechraten beigetragen. So konnten durch Teilnahme der Universitätsklinik Würzburg an einer multizentrischen Studie zur neoadjuvanten Therapie von primär nicht entfernbaren Lebermetastasen (CELIM-Studie) bereits vor einigen Jahren Patienten mit weit fortgeschrittenen Tumorerkrankungen in der Leber einer Leberresektion und damit der Chance auf Heilung zugeführt werden. Abbildung 2 verdeutlicht die signifikante Tumorschrumpfung unter dieser Chemotherapie mittels Computertomographieaufnahmen der Leber vor (links) und 3 Monate nach Chemotherapie (rechts) (rot markiert das Tumorausmaß).
Abb. 2: Resektabilität durch neoadjuvante Therapie
Trotz gewisser Grundstandards muss eine Chemotherapie in Zusammensetzung und Dosis an die jeweilige Tumorerkrankung aber auch an den einzelnen Patienten angepasst werden. Ferner muss der Therapieerfolg in regelmäßigen Abständen z.B. mittels Computertomographie kontrolliert werden. Diesen Therapiearm übernehmen in der Regel Onkologen, die an der Universitätsklinik Würzburg in der Medizinischen Klinik II zu finden sind. (LINK auf KUNZMANN-Abteilung inkl. IOT)
Über das wöchentliche hausinterne interdisziplinäre Tumorboard erfolgt eine enge Vernetzung bzw. Absprache der meist multimodalen Therapiekonzepte (Chemotherapie, Bestrahlung, Embolisation und Operation) zwischen Onkologen, Gastroenterologen bzw. Hepatologen, Radiologen, Strahlentherapeuten, Nuklearmedizinern und Chirurgen, um das optimale Ergebnis durch Einsatz und Kombination dieser verschiedenen Therapieverfahren (Modalitäten) zu erzielen.
Indikation zur Leberresektion
Während noch vor wenigen Jahren die Indikation zur Lebermetastasenresektion sehr eng und vorsichtig gestellt wurden, so ist durch die Ausbreitung und Weiterentwicklung der Resektionstechniken mit der damit verbundenen operativen Routine und Absenkung der OP-Sterblichkeit und OP-Komplikationen die Definition eines resektablen Leberbefundes mittlerweile sehr weit gefasst worden (siehe Abb.3)
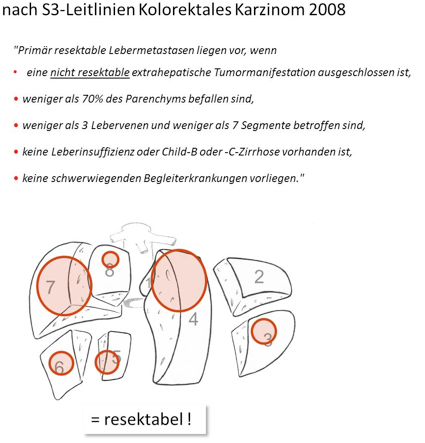
Primär resektable Lebermetastasen liegen vor, wenn
- eine nicht resektable extrahepatische Tumormanifestation ausgeschlossen ist
- weniger als 70% des Parenchyms befallen sind
- weniger als 3 Lebervenen und weniger als 7 Segmente betroffen sind
- keine Leberinsuffizienz oder Child-B oder -C-Zirrhose vorhanden ist
- keine schwerwiegenden Begleiterkrankungen vorliegen
Abb. 3: Definition der Resektabilität nach S3-Leitlinien Kolorektales Karzinom 2008
Präkonditionierung der Leber vor Resektion
Ist trotz Schrumpfung des Tumors durch Einsatz einer Chemotherapie die gesunde zu verbleibende Restleber zu klein (meist liegt dieser Prozentsatz bei 25-30% des ursprünglichen Lebervolumens) kann eine Präkonditionierung bzw. Hypertrophieinduktion (Wachstum durch Regeneration) der Restleber durch Embolisation oder Ligatur des zu resezierenden Pfortaderastes (rechts oder links) erzielt werden (siehe Abb.4).
Um ein ausreichendes Wachstum der Restleber erzielen zu können, muss eine 3-6 wöchige Wachstumsphase eingeplant werden. Sind in beiden Leberlappen Metastasen vorhanden kann eine zweizeitige Leberresektion mit zunächst kleinerer Lebermetastasenresektion auf der zu verbleibenden Seite (meistens linker Leberlappen) und simultaner Pfortaderligatur nach rechts durchgeführt werden. Nach Hypertrophie des meist kleineren linken Leberlappens kann der nun – nur noch arteriell versorgte – rechte Leberlappen nach o.g. Zeitintervall entfernt werden (siehe Abb.5A). Wird im ersten Eingriff bereits das Lebergewebe zwischen rechtem und linken Leberlappen durchtrennt, kann ein signifikanter Hypertrophieeffekt bereits ab dem 10. Tag beobachtet werden (In-situ-Split, siehe Abb.5B)
Abb.5.: Hypertrophieinduktion bei zweizeitigen Leberresektionseingriffen durch Pfortaderligatur. A: klassisches Vorgehen, B: In-situ-Split (modifiziert nach Steger/Germer 2012)
Teilnahme an klinischen Studien bei Lebermetastasen:
– CELIM-Studie I+II (multizentrisch, randomisiert)
Neoadjuvante Chemotherapie vor Leberresektion bei fortgeschrittener bzw. primär inoperabler kolorektalen Lebermetastasierung.
– PANTER-Studie (multizentrisch, randomisiert)
Neoadjuvante versus adjuvante Chemotherapie vor bzw. nach Leberresektion bei primär resektabler kolorektaler Lebermetastasierung (LM). (CET=Cetuximab)





 Lesen Sie weiter auf der Webseite der chirurgischen Univ. Klinik Würzburg...
Lesen Sie weiter auf der Webseite der chirurgischen Univ. Klinik Würzburg...